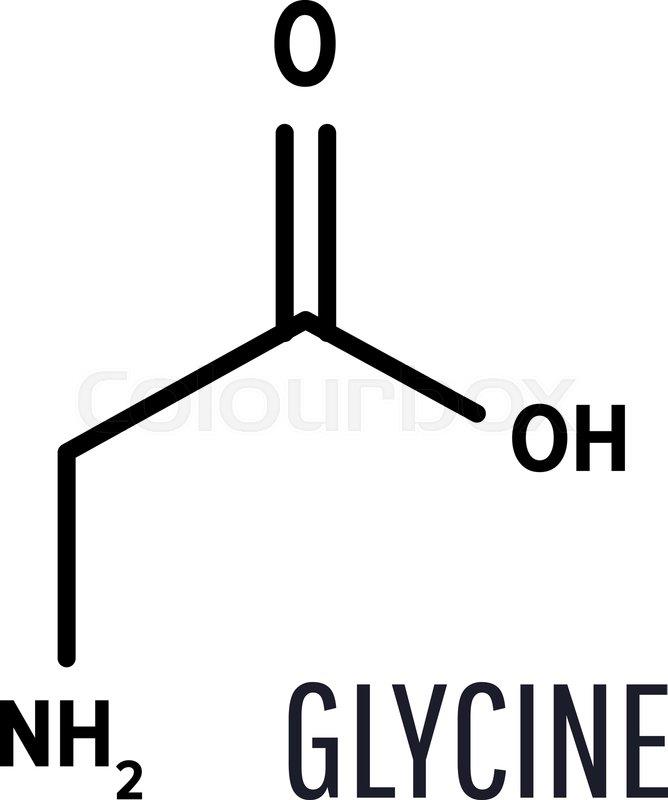
تولید
اگرچه گلیسین را می توان از پروتئین هیدرولیز شده جدا کرد، اما برای تولید صنعتی استفاده نمی شود، زیرا می توان آن را با سنتز شیمیایی راحت تر ساخت.دو فرآیند اصلی آمیناسیون اسید کلرواستیک با آمونیاک، دادن گلیسین و کلرید آمونیوم، و سنتز اسید آمینه Strecker، که روش اصلی مصنوعی در ایالات متحده و ژاپن است. سالانه حدود 15 هزار تن از این طریق تولید می شود.
گلیسین همچنین به عنوان یک ناخالصی در سنتز EDTA تولید می شود که از واکنش های محصول مشترک آمونیاک ناشی می شود.
جهت خرید گلایسین به اینجا مراجعه نمایید.
واکنش های شیمیایی
خواص اسید-باز آن از همه مهمتر است. در محلول آبی، گلیسین به خودی خود آمفوتریک است: در pH پایین، مولکول را می توان با pKa حدود 2.4 پروتونه کرد و در pH بالا، پروتونی با pKa حدود 9.6 را از دست می دهد (مقادیر دقیق pKa به دما و قدرت یونی بستگی دارد).
Glycine-protonation-states-2D-skeletal.png
گلایسین به عنوان یک لیگاند دوتایی برای بسیاری از یون های فلزی عمل می کند. یک کمپلکس معمولی Cu(گلیسینات)2، یعنی Cu(H2NCH2CO2)2 است که هم در ایزومرهای سیس و هم در ترانس وجود دارد.
گلیسین به عنوان یک مولکول دو عملکردی با بسیاری از معرف ها واکنش می دهد. اینها را می توان به واکنش های N-center و carboxylate-center طبقه بندی کرد.
آمین تحت واکنش های مورد انتظار قرار می گیرد. با کلریدهای اسید، اسید آمیدوکربوکسیلیک، مانند اسید هیپوریک[24] و استیل گلیسین به دست میآید. با اسید نیتروژن، اسید گلیکولیک (تعیین ون اسلایک) بدست می آید. با متیل یدید، آمین چهارتایی می شود تا تری متیل گلیسین، یک محصول طبیعی تولید شود:
اچ
3N+
CH
2COO−
+ 3 CH3I → (CH
3)
3N+
CH
2COO−
+ 3 سلام
گلیسین با خود متراکم می شود و پپتید می دهد و با تشکیل گلیسیل گلیسین شروع می شود:
2 اچ
3N+
CH
2COO−
→ اچ
3N+
CH
2CONHCH
2COO−
+ H2O
پیرولیز گلیسین یا گلیسیل گلیسین 2،5-دیکتوپی پرازین، دی آمید حلقوی می دهد.
گلیسین هیدروکلراید نمک هیدروکلریدی است که از ترکیب گلیسین با کلرید هیدروژن ایجاد می شود. این یک ترکیب شیمیایی با فرمول مولکولی C2H6ClNO2 است. به صورت پودر سفید رنگ با نقطه ذوب 176-180 درجه سانتیگراد ظاهر می شود.
منبع
https://en.wikipedia.org/wiki/Glycine